L'angolo del dottorino
Indice
Anemie
Seguici anche sul Blog
Notizie di Attualità su
Salute e Benessere
| OMS & Carne Rossa |
Cannabis Terapeutica | Indice Argomenti |
Cerca nel sito...
Google Ricerca personalizzata

III GRUPPO: EMOGLOBINOPATIE
Il III gruppo delle anemie è chiamato anche gruppo delle emoglobinopatie e racchiude tutta quella serie di anemie dovute a difetti dell’emoglobina.
Si tratta di anemie a carattere ipocromico e microcitico
L’emoglobina è l’effettore molecolare del trasporto dell’ossigeno attraverso il sangue, meno del 2% di ossigeno è presente disciolto in forma libera nel plasma, tutto il resto è legato all'emoglobina.
L’emoglobina è una proteina tetramerica formata da 4 catene globiniche ciascuna delle quali ha una disposizione aminoacidica tale da formare una tasca idrofobica che contiene il gruppo emico proteggendolo dall’ambiente acquoso circostante impedendone l’ossidazione permanente. Il gruppo emico, responsabile del legame reversibile con l’ossigeno, è formato da una proteina chiamata protoporfina IX e ferro bivalente. Il ferro è l’elemento che di fatto lega l’ossigeno ossidandosi a livello polmonare (passaggio dalla forma Fe++ alla forma Fe+++) e riducendosi a livello periferico (passaggio dalla forma Fe+++ alla forma Fe++). L’emoglobina priva di ossigeno viene chiamata desossiemoglobina mentre quella legata all’ossigeno ossiemoglobina. Il numero massino di atomi di ossigeno che una molecola di emoglobina può legare è 4 (avendo 4 gruppi emici presenta 4 siti di legame per l’ossigeno).
Quando tutti i siti di legame per l’ossigeno sono occupati l’emoglobina si dice satura. La percentuale di saturazione dell’emoglobina esprime in percentuale il rapporto tra quantità di ossigeno effettivamente legata all’emoglobina e quantità massima legabile all’emoglobina. (Valori normali tra 95% e 100%).
La quantità di ossigeno legata all’emoglobina è principalmente in funzione della pressione parziale dell’ossigeno dell’ambiente circostante che è massima a livello alveolare dove l’emoglobina si carica di ossigeno (a fronte di una P02 di 100 mmHg c’è una percentuale di saturazione del 98%).
La relazione tra pressione parziale di ossigeno e saturazione di emoglobina è espressa dalla curva di dissociazione dell’emoglobina (immagine qui sotto).
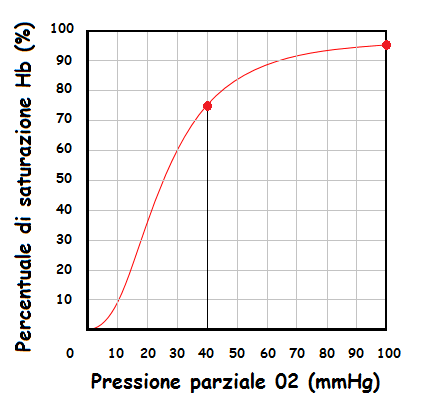
Al diminuire della PO2 diminuisce anche la percentuale di saturazione dell'emoglobina. A livello periferico in prossimità la pressione PO2 è di 40 mmHg a riposo. Come vedete dal grafico alla pressione di 40 mmHg la percentuale di saturazione dell'emoglobina è del 75%, il che vuol dire che in condizioni basali cede una solo molecola di 02 e se ne tiene 3. che vengono rilasciate in caso di aumentato fabbisogno. Alcune condizioni come l'aumento di pressione parziale della Co2, aumento della temperature ed abbassamento del PH (dovuto ad aumento di H+) spostano la curva di dissociazione dell'emoglobina verso destra diminuendone l'affinità per l'ossigeno e favorendo quindi il rilascio dell'ossigeno stesso. Lo spostamento della curva verso destra dovuto all'abbassamento del PH è noto come effetto Bohr. Nelle condizioni di ipossia cronica oltre alle già citate alterazioni di PH e Co2 c'è anche un aumento del 2-3difosfoglicerato (per mancata produzione di ATP) altro fattore che sposta la curva di dissociazione dell'emoglobina. Questo spiega come l'emoglobina sia in grado di compensare l'anemia tramite la maggior cessione di ossigeno, come già accennato nella pagina sulle generalità.
Esistono diversi tipi di emoglobine normali di che differiscono tra loro per le catene proteiche della porzione globinica:
- Emoglobina A (HbA) la forma prinicipale di emoglobina dell'adulto e formata da due catene α e due catene β (α2 β2)
- Emoglobina A2 (HbA2) è anch'essa una emoglobina dell'adulto presente però in una percentuale inferiore al 3% e formata da due catene α e due catene δ (α2 δ2)
- Emoglobina fetale (HbF), presente nella vita fetale (gravidanza dopo i tre mesi) è formata da due catene α e due catene γ (α2 γ2) ed ha una affinità per l'ossigeno rispetto a quella delle emoglobine dell'adulto in modo da garantire il passaggio di ossigeno dal sangue materno (a minore affinità) a quello fetale (a maggiore affinità). In particolari condizioni tale tipo di emoglobina può persistere anche nella vita adulta.
- Emoglobina embrionale (HbE), presente solo ed esclusivamente nella vita embrionale (primi tre mesi di gravidanza) e formata prima da due ζ catene α e due catene ε (ζ 2 ε2) e poi da due catene α e due catene ε (a2 ε2).
Le alterazioni emoblobiniche posso verificarsi sia carico del gruppo emico che della componente globulare, dando quaadri patologichi molto differenti tra di loro
Le principali anemie da emoglobinopatie sono:
- Anemia siderocarenziale: dovuta a mancanza di ferro che è il compontente centrale del gruppo emico che lega l'ossigeno
- Talassemie ed Anemia Mediterranea dovute ad alterazioni qauntitative delle catene globiniche con ridotta o assente produzione di un tipo di catena globinica.
- Anemia Falciforme (o depranocitosi) dovuta ad un'alterazione qualitativa dell'emoglobina.
I contenuti presenti presenti sul sito angolodeldottorino.it sono di proprietà di Moretti Luca, autore e proprietario del sito, e non possono essere copiati,riprodotti,pubblicati o redistribuiti perché appartenenti all'autore stesso. E’ vietata la copia e la riproduzione dei contenuti in qualsiasi modo o forma. E’ vietata la pubblicazione e la redistribuzione dei contenuti non autorizzata espressamente dall’autore.
Copyright © 2015-2016 L'angolo del dottorino by Moretti Luca.
All rights reserved.
Info e contatti: staff@angolodeldottorino.it
All rights reserved.
Info e contatti: staff@angolodeldottorino.it
Dichiarazione di responsabilità:
i contenuti presenti presenti sul sito angolodeldottorino.it sono sono divulgati a scopo informativo e non possono in alcun modo essere considerati sostitutivi della figura di un medico o di altre professioni sanitarie. Informarsi è cosa buona, ma per curarsi e necessario rivolgersi a professionisti della salute. Il proprietario e gli autori di questro sito non possono essere ritenuti responsabili per qualsiasi azione che gli utenti compiono sulla base delle notizie che apprendono su questo sito.